 MOLDE DE
PROTEINAS
MOLDE DE
PROTEINAS Desde la formulación de la molécula de ADN (ácido desoxirribonucleico) en 1953 por Watson y Crick, y el advenimiento de la Ingeniería Genética en 1972, el “gen” representó la clave de la vida, dando origen a la Genómica.
 Mucho se ha
hablado de genes, pero las verdaderas protagonistas son las proteínas.
Mucho se ha
hablado de genes, pero las verdaderas protagonistas son las proteínas. Surge así la PROTEÓMICA.
Ellas son las encargadas de poner en funcionamiento la intrincada maquinaria de los organismos vivos.

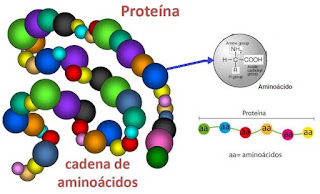
Las proteínas están formadas por sucesiones de aminoácidos, (moléculas compuestas por una parte ácida y otra básica).
El encargado de elaborar esta compleja pared de aminoácidos es el ARN, (ácido ribonucleico), algo parecido al ADN.
Está formado por una simple cadena y un azúcar similar al del ADN, la ribosa en lugar de la desoxirribosa y algunas bases diferentes.
El ARN presenta tres formas distintas, el ARN ribosomal, el ARN de transferencia y el ARN mensajero.
 El ARN mensajero es el encargado de llevar la
secuencia que debe ser decodificada para ensamblar la proteína, operando como
molde.
El ARN mensajero es el encargado de llevar la
secuencia que debe ser decodificada para ensamblar la proteína, operando como
molde. Una investigación de la UBA (Universidad de Buenos Aires), describe por primera vez cómo las proteínas involucradas en esa puesta a punto, al ser modificadas por otras moléculas, influye en la eficiencia con que se realiza el proceso.
Gracias a los investigadores de la Facultad de Ciencias Exactas y Naturales de la UBA, se demostró que cierta modificación en algunas proteínas que intervienen en el armado del molde (ARN mensajero), influye en la eficiencia de ese mecanismo. Si la modificación no se produce, o se realiza de manera anómala, el proceso de corte y empalme se ve impedido.
“Demostramos que cierta modificación de algunas de las proteínas componentes del sistema de corte y empalme (splicing) de ARN, que se denomina spliceosoma, afecta el proceso de splicing”, afirma Anabella Srebrow, investigadora del Instituto de Fisiología, Biología Molecular y Neurociencias (IFIBYNE, UBA-CONICET) y profesora del Departamento de Fisiología, Biología Celular y Molecular de la Facultad de Ciencias Exactas de la UBA.
 La modificación consiste en el agregado
de una pequeña proteína denominada SUMO. Se sabía que ese cambio se producía,
pero se desconocía su importancia para el funcionamiento del spliceosoma.
La modificación consiste en el agregado
de una pequeña proteína denominada SUMO. Se sabía que ese cambio se producía,
pero se desconocía su importancia para el funcionamiento del spliceosoma. “Nosotros mostramos que si esa modificación se ve afectada se altera el proceso de corte y empalme del ARN mensajero, que sirve de molde para la síntesis de proteínas”, comenta la investigadora.
La puesta a punto del ARN mensajero es indispensable para la fabricación de proteínas en el citoplasma de la célula. En el núcleo celular, a través del proceso de transcripción, la información de los genes se transcribe a una molécula de ARN.
Esta molécula tiene que estar acondicionada como para pasar al citoplasma y servir de molde. Debe producirse un proceso de corte y empalme, o splicing, a través del cual se eliminan ciertas porciones del ARN que carecen de información para la fabricación de las proteínas.
“Ese proceso de splicing es complejo, porque hay que cortar pedazos y volver a unir, es como un trabajo de sastre. Esa tarea es realizada por una maquinaria muy compleja, que se llama spliceosoma”, explica Srebrow.
La maquinaria está formada por proteínas y moléculas pequeñas de ARN. “Lo que estudiamos son algunas modificaciones que sufren las proteínas que componen la maquinaria, durante la reacción de splicing”, agrega la investigadora.
Todas las proteínas pueden ser modificadas mediante el agregado de otras moléculas. Esos agregados son indispensables para que la proteína cumpla su función dentro de la célula.
 Una de esas modificaciones es el agregado de la proteína SUMO. El
trabajo, que se publica en Nucleic Acids Research, “describe por primera vez que las proteínas del spliceosoma, al ser
modificadas con las moléculas de SUMO, hacen que el proceso de splicing se
realice de manera diferente, con mayor o con menor eficiencia”, detalla
Berta Pozzi, primera autora del trabajo que también suscribe Laureano Bragado
(tesista doctoral). Ambos son becarios del CONICET en el IFIBYNE.
Una de esas modificaciones es el agregado de la proteína SUMO. El
trabajo, que se publica en Nucleic Acids Research, “describe por primera vez que las proteínas del spliceosoma, al ser
modificadas con las moléculas de SUMO, hacen que el proceso de splicing se
realice de manera diferente, con mayor o con menor eficiencia”, detalla
Berta Pozzi, primera autora del trabajo que también suscribe Laureano Bragado
(tesista doctoral). Ambos son becarios del CONICET en el IFIBYNE. Srebrow comenta: “Ya se conocía que muchas proteínas del splicesoma eran modificadas por la conjugación de SUMO, pero no se sabía si eso tenía alguna consecuencia sobre el proceso de splicing”.
En sus experimentos de laboratorio, los investigadores emplearon un precursor modelo (un fragmento de ARN). En presencia de la maquinaria de splicing, sufre un tipo de corte y empalme determinado. Para ese precursor, encontraron que el agregado de SUMO era necesario para que el proceso se llevara a cabo y se obtuviera el producto final: el ARN listo como molde.

Algunos de los experimentos se realizaron con un extracto del núcleo celular, donde se observaba de qué manera el ARN mensajero pasaba de ser un largo fragmento aún inmaduro, al producto final, el ARN que ya había sufrido el corte y empalme.
Otros experimentos se efectuaron con un cultivo celular, donde se observó cómo, favoreciendo el agregado de SUMO a las proteínas del spliceosoma, la cantidad de ARN maduro aumentaba en relación con las células en las cuales esa modificación no se producía.
“Vimos que si, in vitro, uno altera en forma masiva la modificación de proteínas del spliceosoma, evitando el agregado de SUMO, se altera la eficiencia del proceso”, relata Pozzi y detalla: “Introdujimos en la célula una proteína mutada, a la cual no se le pueden adosar las moléculas de SUMO. Así, pudimos comparar qué pasa en la célula cuando se produce el agregado de SUMO, y cuando este agregado no se realiza”.
El hallazgo resulta de gran importancia puesto que algunas enfermedades se vinculan a mutaciones en los genes a partir de los cuales se fabrican las proteínas del spliceosoma; por ejemplo, algunos tipos de leucemia, y una enfermedad de la retina, la retinitis pigmentosa. En estas patologías, el splicing es defectuoso.
Los genes ya no detentan todo el poder. Lo comparten con las proteínas.
Si las proteínas son modificadas o no por el agregado de otras moléculas, puede dar lugar a diversas patologías.
“Ahora, además del ADN y el ARN, el poder parecen tenerlo las proteínas; éstas poseen una gran diversidad, que en parte se logra a través de su modificación por el agregado o remoción de moléculas. Así se va ampliando la capacidad de un genoma, que con un número limitado de genes da lugar a un número muy amplio de proteínas, a través de estos procesos intermedios que ocurren entre la información que está en el gen y la actividad que va a llevar a cabo cada proteína”, concluye Srebrow.
UBA- Facultad de Ciencias Exactas y Naturales- Julio de 2017


No hay comentarios.:
Publicar un comentario